拉丁美洲拥有约6.5亿人口,占全球总人口8%,城市化率超过80%。其中,巴西是拉美人口最多的国家,有2亿人;墨西哥位居第二,约有1.3亿人。拉美地区的语言构成以西班牙语和葡萄牙语(巴西)为主,覆盖90%以上人口,加勒比海地区则广泛使用英语与法语。区域经济与人口结构持续演进,伴随健康科学和技术领域专业人才的增加,教育普及度不断提升。
再来看该地区的医疗器械市场发展态势。拉丁美洲医疗器械市场呈现稳健增长,驱动因素包括人口增长、医疗保险覆盖范围扩大及先进医疗技术需求攀升。预计拉美医疗器械市场规模将从2024年的450亿美元增至2032年的710亿美元,复合年增长率达5.8%。巴西、墨西哥、哥伦比亚为区域核心市场,阿根廷亦具显著潜力。这几个国家的战略优势体现在市场规模、竞争力、贸易协定及相对简化的监管流程,为国际企业进入创造有利条件。
巴西:作为区域最大医疗市场,对进口医疗器械需求旺盛。国家卫生监管局(ANVISA)是区域最大的卫生部门,致力于推进国际监管协调,以优化产品审批流程。私人医疗投资不断增长,推动对先进医疗技术的需求。
墨西哥:拉美第二大市场,对高品质进口器械存在刚性需求。联邦卫生风险保护委员会(COFEPRIS)是墨西哥卫生部下属的一个监管机构,负责医疗器械市场准入与合规监管。人口老龄化与慢性病负担加重持续刺激墨西哥医疗创新需求。
哥伦比亚:区域内增长迅速且规模第三的医疗器械市场。作为安第斯地区及泛拉美市场的门户,区位优势明显。国家食品和药品监督局(INVIMA)主要遵循国际标准构建监管框架,以促进市场准入。哥伦比亚已签署逾60项贸易协定,助力企业通达整个拉美市场。
一、该地区未来发展趋势与机遇
- 一是数字健康扩展:远程医疗在远程护理数字解决方案中的应用快速增长;
- 二是监管协调:趋势正朝着跨重点市场的统一监管流程发展,如南方共同市场(阿根廷、智利、巴西、巴拉圭、乌拉圭)和太平洋联盟(智利、哥伦比亚、哥斯达黎加、墨西哥);
- 三是价值医疗:对通过科技改善健康结果和成本效益优化的需求持续;
- 四是可持续聚焦:对环保和可持续医疗设备的偏好增强;
- 五是公私协作:政府与私营部门合作深化,加速医疗基础设施现代化进程;
- 六是上市后监管加强:技术警戒与法规遵从要求日趋严格;
- 七是家庭护理市场增长:便携式设备与家庭护理市场显著扩张。
二、对于中国制造商的战略机遇
- 一是拉美医疗设备市场在人口和现代化需求驱动下持续扩张;
- 二是多个国家正优化监管路径,创造加速市场准入机会,这些机会尤其体现在诊断设备、家庭护理及可穿戴设备等细分领域;
- 三是随着中产阶级崛起,购买力提升及对先进医疗解决方案的需求增长;
- 四是区域贸易壁垒与进口关税逐步降低。
同时,中国产品在创新、质量提升与市场信任度方面声誉良好,尤其在新能源汽车等领域的成功经验可产生积极外溢效应。
三、重点进口医疗器械类别(按国别)
巴西:影像诊断设备(如磁共振成像和CT扫描仪)、生命体征监测仪、呼吸机或雾化器等呼吸治疗设备、手术器械和血液透析装置。
墨西哥:自动调节和控制仪表、手术剪镊部件及附件、眼镜镜片和导管。
哥伦比亚:生命体征监测仪、呼吸机及麻醉设备、手术台和培养箱。这些新兴趋势带来了激动人心的机遇,同时也伴随着法规监管和战略挑战。在拉美每个市场,通常有多个权威机构来监管医疗设备。卫生部通常负责发布法规,而ANVISA(巴西)、COFEPRIS(墨西哥)或INVIMA(哥伦比亚)等机构则负责授予产品许可证或上市授权以及进行监管。此外,还有其他权威机构,例如保护消费者免受误导性广告影响的工商监管局。
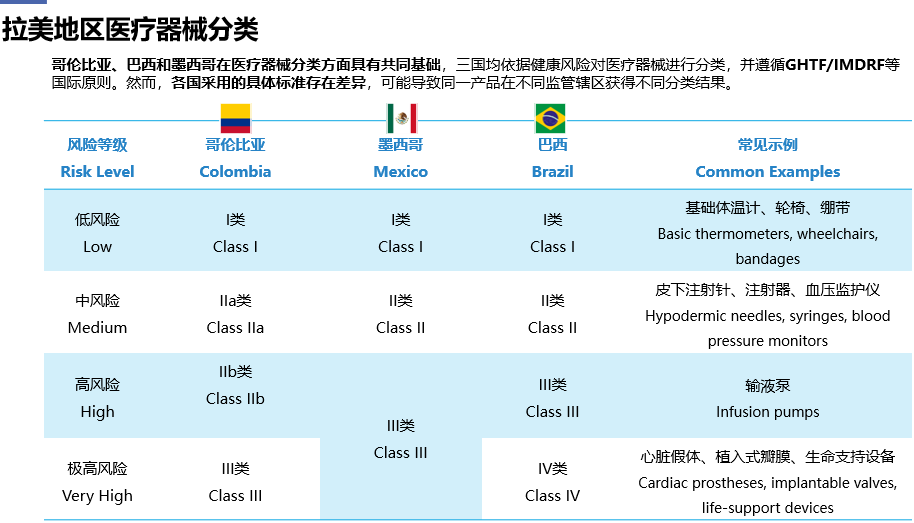
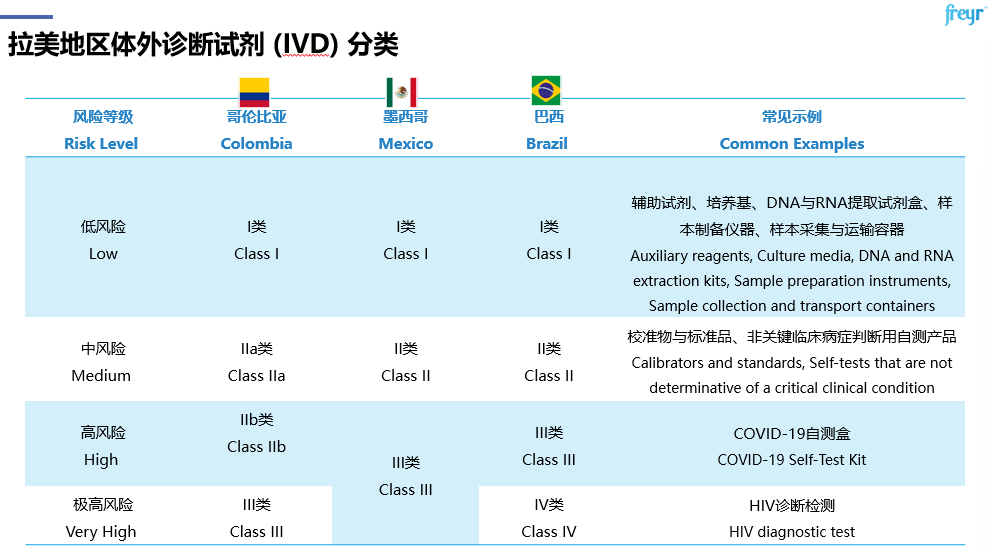
对于医疗器械的分类问题,哥伦比亚、巴西和墨西哥等国家在医疗器械分类上具有共同基础,主要依据健康风险对医疗器械进行分类,并遵循GHTF/IMDRF等国际原则。然而,各国采用的具体标准存在差异,这可能导致同一产品在不同辖区的分类差异。下图中提供了每个类别的常见示例供参考。此外,体外诊断(IVD)产品亦依据风险进行分类,这些国家在这方面亦有共同之处。
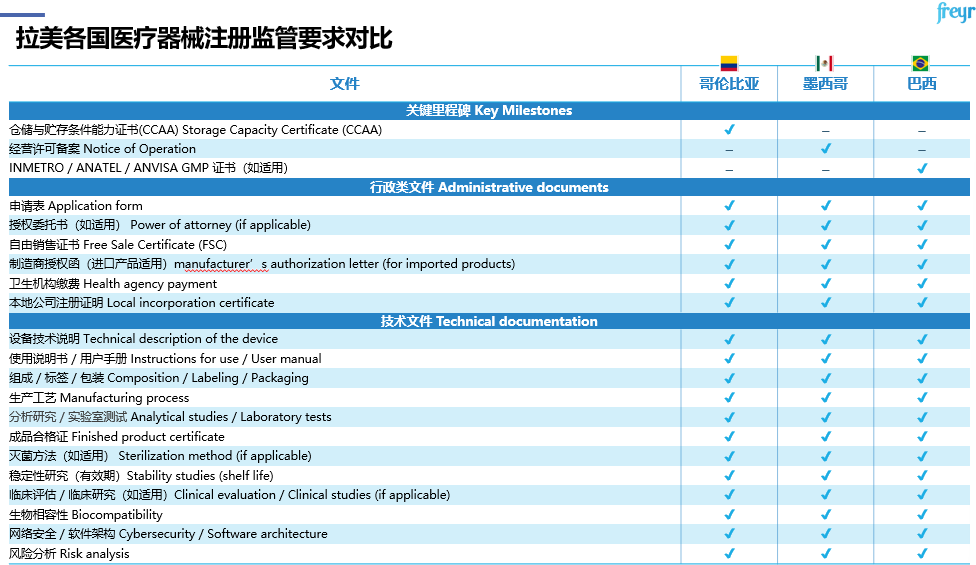
对于产品注册监管要求,尽管每个国家均设有其特定的注册要求,例如哥伦比亚的CCAA证书、墨西哥的经营许可备案,以及巴西的INMETRO或ANATEL认证,但行政和技术要求大体相似。此外根据产品健康风险的不同,相关文件可能会受到更为严格的审查。
四、关于注册要求与时限
巴西:I/II类器械的注册通知后大约需时30天;III/IV类器械的注册则大约需要320天,IVD的注册周期约为一年。该过程受卫生当局工作量的影响较为显著。
哥伦比亚:器械注册所需时间约为三个月。
墨西哥:法定的注册周期为60个工作日,但实际操作中,整个周期可能延长至8个月。
五、关于注册证的有效期及续证事宜
巴西:III/IV类器械的注册证有效期为10年,并且可以续期;I/II类器械则无需进行再验证即可豁免。
哥伦比亚:器械注册证有效期为10年,并且可以续期。
墨西哥:器械注册证有效期为5年,并且可以续期。
六、续证截止期限与要求方面
巴西的注册证到期前6-12个月提交。
哥伦比亚和墨西哥,可以在到期前提交。续约要求通常比初次提交时简化,主要侧重于更新文件和信息。
在探讨各国市场时,企业通常会遭遇若干挑战。
巴西对于创新医疗器械的监管体系颇为严格,企业需遵循详尽的法规框架,涵盖产品分类、ANVISA颁发的GMP认证、INMETRO及其他认证。此外,葡萄牙语的标签和使用说明,以及创新或高风险设备的临床证据是不可或缺的。
哥伦比亚市场的主要挑战在于企业必须指定一位具备特定经验的当地法定代表人,该代表需对哥伦比亚市场及所注册产品类别有深入了解。进口商必须获得仓储和储存能力证书(CCAA证书),这是向INVIMA提交注册申请的必要文件。
墨西哥市场也面临着各种挑战。例如,设备分类可能因原产国而异,同时墨西哥严格的法规又限制了组合注册,因此设备必须单独注册并可能导致注册成本增加。此外,COFEPRIS的审批流程较长,且缺乏针对创新技术(如医疗人工智能)的监管框架。
在我们对市场前景和监管框架有了清晰的了解之后,成功战略的下一步是将关键洞察与重点市场准入相结合。
(来源:中国医药保健品进出口商会,作者:Mario Duque)




